Empat Pilar – Perbedaan Anoda dan Katoda Secara Lengkap : Pahami dengan Baik. Temukan perbedaan anoda dan katoda secara lengkap dalam artikel ini. Pelajari sejarah, konsep, dan aplikasi praktis dari dua kutub penting dalam elektrokimia.
Dalam dunia elektrokimia, terdapat banyak istilah yang mungkin awam bagi sebagian orang. Salah satunya adalah anoda dan katoda.
Meskipun kedua istilah ini sering digunakan dalam kehidupan sehari-hari, banyak yang masih belum mengerti perbedaan anoda dan katoda secara lengkap.
Di sinilah kita akan membahas topik ini secara mendalam, menjelaskan sejarah, konsep, dan aplikasi praktis dari kedua istilah ini.
Untuk memahami perbedaan anoda dan katoda secara lengkap, kita perlu melihat sejarahnya terlebih dahulu.
Anoda dan katoda pertama kali diperkenalkan oleh ilmuwan Inggris, Michael Faraday, pada abad ke-19.
Faraday melakukan eksperimen dengan sel elektrokimia dan menciptakan istilah anoda dan katoda untuk menggambarkan dua kutub yang berbeda dalam sel tersebut.
Pengertian Anoda
Anoda adalah elektroda di mana arus konvensional mengalir ke dalam perangkat listrik yang terpolarisasi.
Elektroda ini berbeda dengan katoda, yang mana arus konvensional meninggalkan perangkat listrik.
Ada sebuah mnemonik umum yang mengatakan “arus anoda ke dalam perangkat”. Arah arus dalam rangkaian berlawanan dengan arah aliran elektron.
Oleh karena itu, elektron bermuatan negatif mengalir keluar dari anoda pada sel galvanik, menuju sirkuit eksternal yang terhubung ke sel tersebut.
Dalam sel galvanik dan sel elektrolitik, anoda adalah tempat terjadinya reaksi oksidasi.
Pada sel elektrolisis, anoda merupakan kawat dengan muatan positif. Anion cenderung bergerak menuju anoda, di mana mereka kemudian dapat mengalami oksidasi. Secara historis, anoda juga dikenal sebagai zincode.
Contoh Anoda
Anoda adalah terminal negatif pada pemakaian baterai atau sel galvanik karena di sinilah arus mengalir ke dalam sel. Arus ini dibawa oleh elektron yang bergerak keluar. Muatan negatif yang mengalir dalam satu arah sama dengan muatan positif yang mengalir dalam arah yang berlawanan.
Pada baterai isi ulang, anoda menjadi terminal positif yang menerima arus dari generator eksternal. Arus yang melalui baterai berlawanan dengan arah arus selama pengosongan baterai yang sedang diisi ulang. Secara sederhana, elektroda yang merupakan katoda saat pengosongan baterai menjadi anoda saat baterai sedang diisi ulang.
Dalam dioda, anoda menjadi terminal positif tempat arus mengalir ke perangkat. Penamaan elektroda untuk dioda didasarkan pada arah arus maju.
Sedangkan pada tabung vakum atau tabung berisi gas, anoda menjadi terminal sementara arus masuk ke dalam tabung.
Pengertian Katoda
Katoda adalah elektroda pada perangkat listrik terpolarisasi yang menjadi tempat arus listrik meninggalkan perangkat.
Kata “katoda” sendiri berasal dari bahasa Yunani yaitu “kathodos” yang berarti “jalan keluar”.
Dalam mengingat kembali fungsi katoda, dapat digunakan mnemonic “Cathode Current Departs”. Hal ini berarti bahwa arus listrik yang keluar dari perangkat melewati katoda.
Namun, penting untuk diingat bahwa arus konvensional menunjukkan arah pergerakan muatan positif.
Sedangkan elektron memiliki muatan listrik negatif. Oleh karena itu, pergerakan elektron di dalam katoda sebenarnya berlawanan dengan arah aliran arus.
Secara umum, katoda digunakan pada berbagai perangkat elektronik, seperti dioda, tabung sinar katode, dan bahkan pada baterai.
Pada dioda, katoda menjadi terminal negatif di mana elektron mengalir keluar dari perangkat. Sementara pada tabung sinar katode, elektron dipancarkan dari katoda dan dipercepat menuju ke anoda oleh medan listrik.
Sedangkan pada baterai, katoda menjadi terminal negatif di mana elektron mengalir keluar dari baterai dan ke perangkat yang membutuhkan listrik.
Contoh Katoda
Arus katodik adalah aliran elektron yang terjadi dari antarmuka katoda ke spesies dalam larutan. Arus ini memainkan peran penting dalam berbagai jenis sel elektrokimia, seperti yang dijelaskan di bawah ini:
1. Sel Elektrolisis
Dalam sel elektrolisis, katoda berfungsi sebagai tempat penerapan polaritas negatif. Beberapa hasil reduksi yang terjadi di katoda berupa logam murni atau gas hidrogen dari ion logam.
Ketika mempelajari kekuatan reduksi relatif dari dua agen redoks, pasangan yang menghasilkan spesies yang lebih banyak direduksi akan lebih katodik dibandingkan dengan reagen yang lebih mudah direduksi.
2. Sel Galvani
Dalam sel galvani, katoda menjadi kutub positif. Kutub positif ini terhubung untuk memungkinkan sirkuit selesai.
Anoda sel galvani mengeluarkan elektron dan kembali dari sirkuit ke dalam sel melalui katoda.
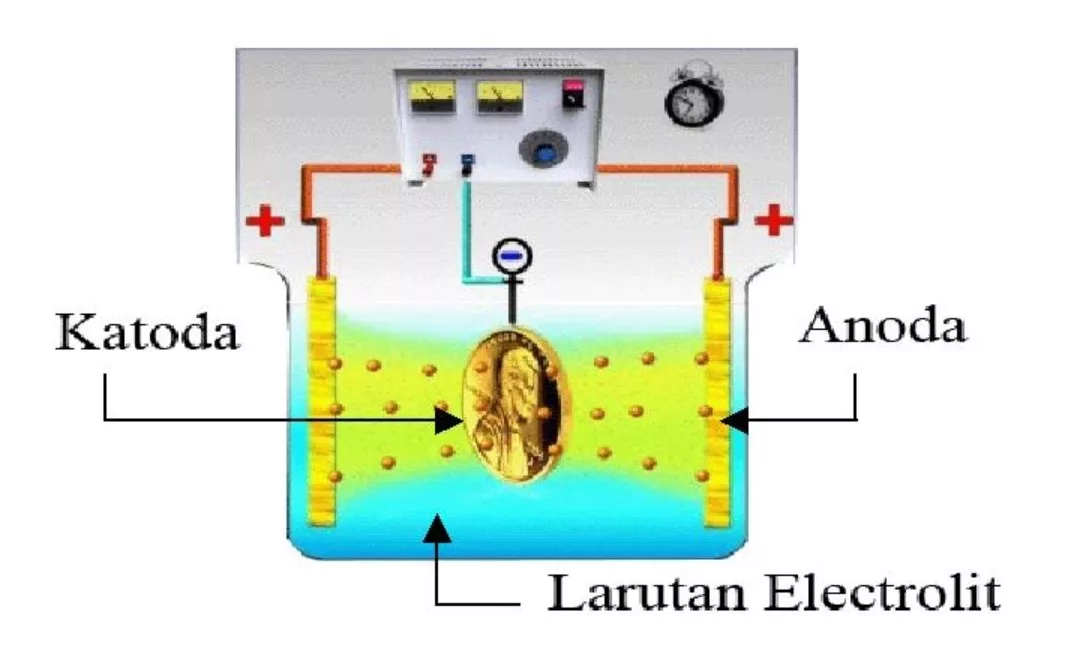
3. Elektroplating dengan Menggunakan Katoda dari Logam
Dalam proses elektroplating logam, ion logam direduksi dan membentuk permukaan logam murni pada katoda.
Benda yang akan disepuh dengan logam murni dilekatkan dan menjadi bagian katoda dalam larutan elektrolit.
Dalam semua jenis sel elektrokimia ini, arus katodik terlibat dalam proses reduksi dan pemurnian bahan kimia, serta digunakan untuk menghasilkan arus listrik dalam sel galvani.
Perbedaan Anoda dan Katoda
Nah berikut adalah beberapa Perbedaan Anoda dan Katoda, secara lengkap dan jelas yang perlu kalian pahami :
- Faktor kunci yang membedakan antara anoda dan katoda adalah bahwa anoda sesuai dengan elektroda di mana oksidasi terjadi, yaitu kehilangan elektron. Sedangkan katoda sesuai dengan elektroda di mana reduksi terjadi, yaitu mendapatkan elektron.
- Namun, denotasi spesifik anoda sebagai positif dan katoda sebagai negatif tidak selalu benar. Hal ini terjadi karena polaritas terminal bervariasi tergantung pada jenis sel elektrokimia yang digunakan, yaitu elektrolisis atau galvanik.
- Untuk sel elektrolisis, anoda bertindak sebagai terminal positif, sementara katoda memegang polaritas negatif. Oleh karena itu, di sini anoda menarik partikel bermuatan negatif, sedangkan katoda menarik partikel bermuatan positif.
- Sedangkan untuk sel galvanik, anoda memegang polaritas negatif, sedangkan katoda bertindak sebagai terminal positif. Oleh karena itu, di sini anoda akan menarik partikel bermuatan positif dan katoda akan menarik partikel bermuatan negatif.
Dalam praktiknya, anoda dan katoda digunakan dalam berbagai perangkat elektrokimia, seperti baterai, dioda, dan sel elektrolisis.
Anoda dan katoda sering digunakan bersama-sama dalam rangkaian sirkuit untuk menghasilkan arus listrik.
Oleh karena itu, pemahaman yang tepat tentang perbedaan antara anoda dan katoda sangat penting untuk memahami prinsip kerja perangkat elektrokimia.
Perbedaan Anoda dan Katoda
Setidaknya terdapat perbedaan utama antara anoda dan katoda, antara lain :
| No | Perbedaan | Anoda | Katoda |
|---|---|---|---|
| 1 | Hubungan dengan elektroda | Anoda berhubungan dengan elektroda dimana oksidasi (kehilangan elektron) terjadi | Katoda berhubungan dengan elektroda dimana reduksi (penguatan electron) terjadi |
| 3 | Sel elektrolitik | Anoda bertindak sebagai terminal positif | Katoda memegang polaritas negatif |
| 3 | Sel galvanik | Anoda memegang polaritas negatif | Katoda bertindak sebagai terminal positif |
Fungsi Anoda dan Katoda
Terkait dengan kegunaan dan fungsi anoda dan katoda, berikut adalah penjelasan yang dapat dijabarkan:
1. Anoda
Anoda berperan sebagai elektroda yang memiliki muatan positif. Fungsi utamanya adalah menarik elektron atau anion.
Dengan demikian, anoda menjadi sumber muatan positif atau penerima elektron.
Anoda seringkali digunakan pada berbagai aplikasi, seperti pada sel elektrokimia, tabung sinar katode, atau dalam proses elektroplating.
2. Katoda
Katoda merupakan elektroda yang memiliki muatan negatif. Fungsi utamanya adalah menarik kation atau muatan positif.
Sebagai elektroda yang mampu mendonorkan elektron, katoda menjadi sumber dari arus elektron yang mengalir dari arah katoda ke anoda.
Katoda banyak digunakan dalam berbagai aplikasi, seperti pada sel elektrokimia, tabung sinar katode, lampu neon, atau dalam proses las listrik.
Dalam banyak kasus, anoda dan katoda bekerja secara bersama-sama dalam suatu sistem.
Anoda dan katoda ini akan membentuk sebuah sirkuit listrik yang dapat digunakan untuk berbagai macam aplikasi, seperti pada baterai, sel surya, atau proses elektrolisis.
Dalam proses-proses ini, anoda dan katoda seringkali digunakan untuk memisahkan muatan positif dan negatif serta untuk mendapatkan energi listrik dari perbedaan potensial antara kedua elektroda tersebut.
Kesimpulan
Dalam rangkuman ini, empatpilar.com telah membahas perbedaan anoda dan katoda secara lengkap, mulai dari definisi, fungsi, hingga peran mereka dalam berbagai aplikasi.
Anoda dan katoda adalah dua elemen penting dalam berbagai sistem elektrokimia, seperti baterai, sel elektrolisis, dan banyak lagi.
Perbedaan utama antara anoda dan katoda adalah kutub mereka, di mana anoda merupakan kutub positif yang menarik ion negatif, sedangkan katoda merupakan kutub negatif yang menarik ion positif.
Selain itu, proses oksidasi terjadi pada anoda, sementara reduksi terjadi pada katoda. Pemahaman yang baik tentang perbedaan ini penting untuk memahami prinsip kerja berbagai perangkat dan proses elektrokimia.
Semoga artikel ini memberikan pengetahuan yang bermanfaat mengenai perbedaan anoda dan katoda secara lengkap.
Dengan pemahaman yang lebih baik tentang konsep dasar ini, kita dapat lebih menghargai teknologi yang ada di sekitar kita dan juga berkontribusi dalam pengembangan teknologi yang lebih efisien dan ramah lingkungan di masa depan. Kata Pencarian Terpopulerhttps://www empatpilar com/perbedaan-anoda-dan-katoda/